
抗肿瘤新药已在国外上市,但大量中国患者就是没法吃上。因为,这些药还没在中国上市。是什么卡住了这些“救命药”在国内使用的步伐?与死亡赛跑,让这些患者多一份生机与希望,上海多个部门全力以赴,行动起来。
由于该事项涉及药监、卫生、海关等多系统,需多方协作推进,上海市食药监主动出击,深入多部门调研。今天,记者从上海市食药监局获悉,在本市指定医疗机构定点先行使用国外已上市抗肿瘤新药的试点工作方案已形成,也在与国家药监等相关部门沟通,希望在政策允许的情况下有所突破,让中国肿瘤患者不再“望药兴叹”。
能否改变“人等药”的历史?
“海外抗肿瘤药在国内上市,患者的呼声很高,真的是‘救命药’,但我们现在的制度上还存在这样、那样的障碍。”上海市食药监局副局长陈尧水坦言。
确实,近年来,我们身边出现了这样的情况:为了吃上国外已上市、国内买不到的新药,一些晚期肿瘤患者通过中介出境看病、通过网上跨境购药或请人携带药品入境。但依据我国药品管理相关办法,在国内生产、销售、使用未在我国批准上市的药品,一律以假药论处。如此违法购买“假药”的现象,为患者带来治疗甚至救命希望,也存在诸多安全隐患、法规风险。

但,“救命”的需求活生生摆在那里。此前有媒体报道,有患者甚至不顾风险根据公开的配方,通过互联网找到一些药粉,配上淀粉,用天平称重量,放在胶囊里自行服用。“这种药没有经过任何的临床试验,患者甘愿冒着生命危险去吃这种原料药。”某海外药品代购这样说。
“以前,我们更多从安全性考量,鉴于不同人种的药物代谢差异,国外已上市药物在我国患者使用过程中可能产生不同的效果和反应,因此需要有足够的亚洲人种临床研究数据,才能通过我国药监部门的技术审评并批准在国内上市。”陈尧水分析,这样一来,就存在“人等药”的问题。
对肿瘤患者尤其晚期肿瘤患者来说,病情瞬息万变,分秒必争,如何让他们尽快用上国外抗肿瘤新药?如何既保证百姓急需用药又保证安全?过去几周,上海市食药监局带着这个问题密集调研,走访上海的卫生、海关等相关系统,希望多方协同“求突破”。
考虑将医疗机构作为申请主体
目前,市食药监局已形成在本市指定医疗机构定点先行使用国外已上市抗肿瘤新药的试点工作方案和一系列风险控制措施。
调研中,他们发现,现在的方案还存在几个问题:此类药品未在国内上市,该如何定价?药品在购进、运输、储存等环节由谁具体负责?该由谁来提出进口药品申请?使用过程中,又有谁来确保安全?
“毕竟它是没有经过我们国内注册评价的,我们既看到要突破,同时能有一个严格的风险防控对策。”陈尧水称,包括“谁提出、谁审批、谁提供,如何监管,如何使用”等,对这个新方案相关的一步步都要有所考量。
业内专业人士清楚,患者不能直接使用国外药物,这是国际惯例,主要就是基于人种差异带来的用药风险。以心血管药物普萘洛尔(心得安)为例,若要使患者的心率下降20%,所需要的药量黄种人比白种人低一半左右,也就是说,同样的剂量,美国人用起来刚好,中国人则可能因过量而出现严重不良反应。临床验证和技术审评是保护人民用药安全的有效途径,但需要一定的时间,这就造成了国内、国外新药上市的时间差。
记者获悉的方案内容包括:首先,由医疗机构作为申请主体,市食药监局联合市卫计委,综合医院能级、医疗服务、质量管理水平和临床使用经验等因素,指定具备肿瘤专科特长的综合性医院和学科排名位于全国前列的科室作为指定试点单位。
其次,市卫计委会同市食药监局拟定具体品种目录,在指定医疗机构,探索性地使用已被美国、欧盟、日本等地区的药品监管机构批准上市,但在我国尚无同品种产品获准注册的国外抗肿瘤新药,用于在现有诊疗规范下无更多可供选择的治疗手段的晚期肿瘤患者。
在合法合规的前提下“吃上药”
记者注意到,初步方案十分强调“风险可控”。市食药监局对此事的态度很明确:听到了大量患者的需求,主动推动,希望有所突破,但如何把风险控制到最小是同时要考虑的。
“这个方案是针对临床特别急需、且没有治疗手段的危重病人,我们现在的想法是限制品种、固定到品种,包括固定到临床医生,归根结底我们要做到整个过程的可控,包括前期医生给出的治疗方案、伦理委员会的通过、用药患者的知情同意、用药后的不良反应监测、每个病人的追踪等。”上海市食药监局药品注册处处长张清称。
此前,国家药品相关条例有提到,对临床少量急需、自用的是可以进行申请以后报批进行进口。不过,业内也谈到,它的实际应用中依然需要审批,存在“时间差”的问题,而“人等药”的情况就让不少患者可能错过最佳治疗时期,对晚期肿瘤病人来说,时间就是生命。
“我们希望在合法合规的框架下,让患者尽快吃得上救命药。”市食药监局表示,将进一步会同相关部门修改、完善试点方案,并积极争取国家相关部门的支持,着力解决恶性肿瘤患者的用药问题。
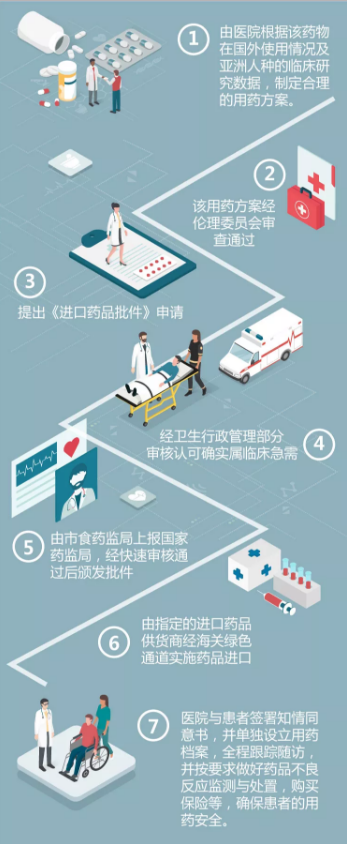
▲为让患者尽快吃上进口肿瘤药,上海市食药监局经多部门调研形成初步方案。
作者:唐闻佳
编辑:李晨琰
责任编辑:李雪林
*文汇独家稿件,转载请注明出处。





