相关文章
推荐文章
排行榜
细胞免疫治疗中国创新再下一城!张江药企美国血液病学会年会上公布最新临床数据
日期:2019年12月06日 16:51:35 作者:唐玮婕

药明巨诺中国今天在第61届美国血液病学会年会上公布其首个在研产品JWCAR029的一期临床试验的数据,治疗成人B细胞非霍奇金淋巴瘤的CAR-T产品显示了良好的安全性和有效性,临床的总缓解率、完全缓解率和毒副发生率都达到国际先进水平。
这是中国国内首个在国家药品监管局药品审评中心(CDE)新药研究申请(IND)批准下的细胞治疗产品的临床数据发布。药明巨诺方面透露,已启动商业化布局,推进JWCAR029 CAR-T在研产品的产业化进程,早日让更多的患者从中受益。
JWCAR029是药明巨诺在美国巨诺公司开发的JCAR017基础上研发的国家一类创新生物药,并获得了中国首个以CD19为靶点的CAR-T细胞治疗药物的IND临床批件。在一期临床的基础上,公司目前进行中的二期临床试验,旨在扩大人群中进一步评估JWCAR029在治疗成人复发/难治B细胞非霍奇金淋巴瘤(R/R B-NHL)患者中的安全性和有效性。与此同时,公司也正陆续开展JWCAR029其它血液肿瘤适应症的临床研究。
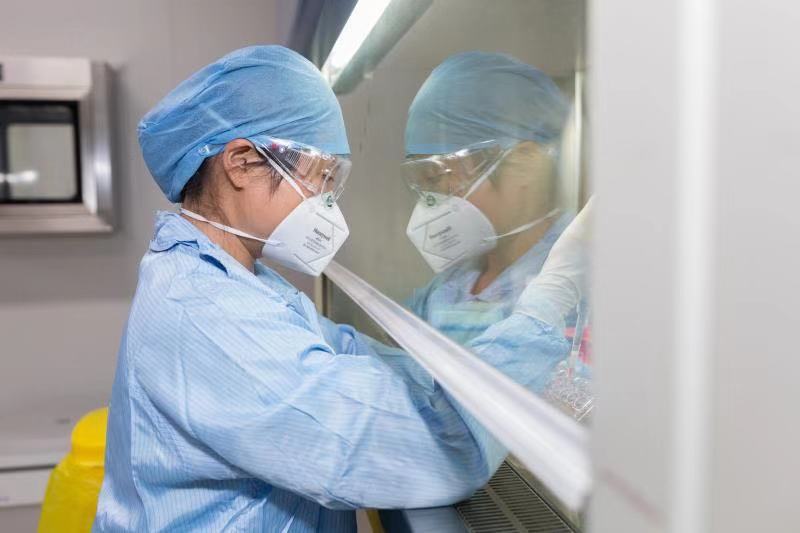
作为一家专注于细胞免疫治疗的研发、转化及应用,处于临床阶段的创新型生物医药公司,药明巨诺中国正致力于与国内外合作伙伴携手打造国际领先的细胞免疫治疗技术创新平台,共建行业规范与生态系统,引领细胞免疫治疗的全面发展,造福更多的患者。
作者:唐玮婕
编辑:王翔
责任编辑:邵珍
*文汇独家稿件,转载请注明出处。
文汇网 ● 版权所有 All Rights Reserved ICP许可 沪 B2-20150001 号 Copyright(c)2004 沪公网安备 31010602000205号





