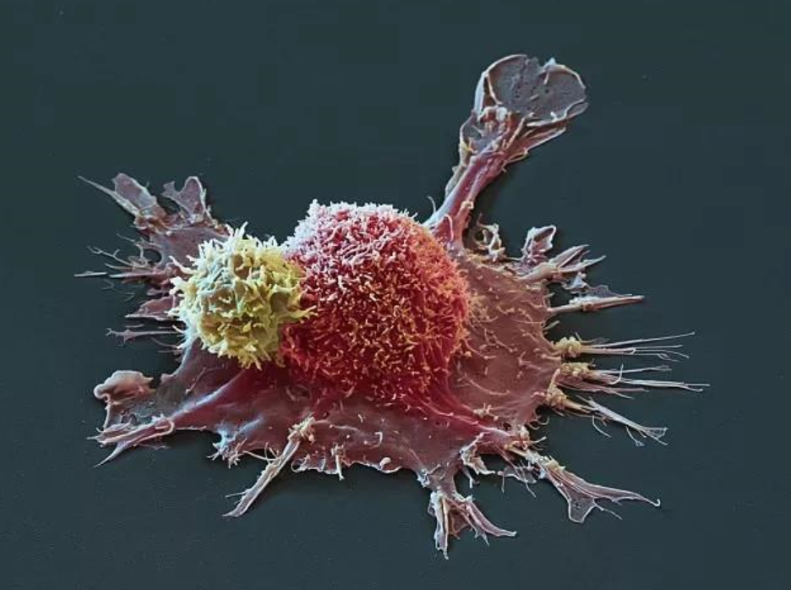
▲放大2600多倍的CAR-T细胞(黄色)攻击癌细胞(红色)的图像
肿瘤免疫疗法如火如荼,CAR-T成为肿瘤免疫治疗的新手段之一。
2012年迄今,CAR-T多次上演奇效,全球有超过25个研究中心证实其治疗白血病、淋巴瘤等疾病的有效性。2017年12月,中国首个CAR-T临床试验申请获药监部门受理,一年多来,备受关注。
那么,到底这种创新疗法走到了哪一步,又是什么肿瘤患者有望从中获益呢?3月9日-10日,嘉会国际医院肿瘤中心联合美国麻省总医院癌症中心在沪主办“肿瘤创新疗法前沿大会—淋巴瘤与骨髓瘤的研究、实践、指南”大会,中美医学专家在分享CAR-T等肿瘤前沿疗法最新进展的同时强调:CAR-T并非人人适用,全程副反应管理将成为重点。
CAR-T是一种细胞免疫疗法,利用人体免疫细胞来清除癌细胞,作用流程是先从癌症患者身上分离出其自身的免疫T细胞,在体外用基因工程改造的方式给它带上一个“子弹头”,然后将带有“子弹头”的CAR-T细胞回输到病人体内。进入体内后,CAR-T细胞将大量扩增,消灭癌细胞。
据嘉会国际肿瘤中心副主任周莉莉教授介绍,截至目前,全球共计54项骨髓瘤领域CAR-T研究中,美国占26项,中国占24项。中美两国学者在CAR-T研究的世界舞台上起到的引领作用,可窥一斑。
CAR-T研究、临床申请如火如荼,且亦有个案报道其在临床上显示较好疗效,与会专家仍希望提醒公众:科技进步鼓舞人心,但CAR-T研究尚在早期,还需相当数据和经验的积累,建议患者选择时不要“一窝蜂”。
嘉会国际医院肿瘤中心主任陈健行谈到,患者首先需要学会区分“批准”和“研究”的差别。目前,就国际上而言,CAR-T被批准的适应症只在淋巴瘤和白血病,在其他病种上的突破性进展尽管令人兴奋,但还都属于“研究性质”。

美国麻省总医院多发性骨髓瘤中心主任Noopur RAJE教授透露,在骨髓瘤领域的CAR-T临床研究中,全球总共已有200例患者入组,麻省总院参与其中近30例,这些病例主要集中在复发难治性患者。
“他们往往已接受过既往7-8线的治疗,也就是说,对现有治疗方法全部失败,才被纳入CAR-T临床实验。”她强调,还需要积累更多病例数据来研究CAR-T治疗中至关重要的副反应发生情况,以便对其加以全程管理、控制,才能将治疗对患者的风险降到最低,获益升至最高。
对CAR-T这类创新技术,能否真正让患者获益,全程副反应管理成为医生关注的焦点。
“CAR-T是细胞,不是药。”血液科医生解释,其在人体内引起的炎症型副反应——细胞因子释放综合征(CRS)表现为体内所有细胞因子骤然升高,有可能导致病人突然发烧、低血压、严重神经毒性反应导致认知障碍等情况。
不过,这些副反应是可管理的。美国麻省总院分享经验显示,在已完成的CAR-T临床试验中,1-1.5年间总体有效率高达90%,神经副作用发生率不足1%,严重CRS发生率仅30%,且均获得有效控制。
也基于此,对副反应的全程监测、识别、早期用药干预、调控及后续长期随访对应用这类新技术的医生而言变得越来越重要,因为,这可能改变甚至影响CAR-T的治疗效果。
就患者是否不必住院,在门诊即可接受CAR-T治疗这一问题,美国麻省总医院癌症中心淋巴瘤中心临床主任Jeremy Abramson教授回应称,每种CAR-T细胞不同,结构和毒性不同,疗效也不同,想在门诊完成CAR-T治疗并非不可能,但必须满足一些条件:
第一,它不导致细胞因子释放综合征(CRS)、不导致神经毒性;
第二,导致的CRS或神经毒性是迟发的,也就是在输入后过几天才出现;
第三,导致的CRS或神经毒性不严重,不会使病人需要进入重症监护室抢救的程度,换言之,给予医生有调控其副反应的时间、空间。
据了解,国内尚未有CAR-T正式获准上市,现有开展的CAR-T项目均为临床试验。
上海嘉会国际医院表示,不仅共享有麻省总医院在CAR-T副反应管理方面的经验,也可提供相关血液肿瘤患者以国际会诊、转诊或参与海外临床试验方式,获得包括麻省总院在内的多家海外医疗机构的CAR-T治疗机会。
不过,院方强调“送出国门”并非第一考量,而是将与中外合作医院、医学院专家慎重考量患者是否需要、且适用该新疗法,并全程参与治疗的病史整理、中期沟通、后期随访及回国后的医疗处理。
作者:唐闻佳
编辑:沈湫莎
责任编辑:顾军
*文汇独家稿件,转载请注明出处。





